Pnei e fegato


I batteri “buoni” che risiedono nel nostro tratto gastrointestinale possono proteggerci dall’infiammazione, mentre la loro distruzione (disbiosi) può aumentare la suscettibilità del fegato a forme più dannose di malattia come la steatosi epatica non alcolica. Per questo motivo in ambito Pnei e fegato, la metodologia Pneisystem prevede da sempre la cura del microbiota e mirata integrazione ove necessario.
E sempre in ambito Pnei e fegato, uno studio, ora disponibile sulla rivista Cell Reports, ha identificato due metaboliti chiave prodotti dai batteri nei topi che modulano l’infiammazione nell’ospite e potrebbero infine ridurre la gravità della steatosi epatica non alcolica.
La steatosi epatica non alcolica (NAFLD) è una condizione prevalente nei paesi occidentali e colpisce fino al 25% degli adulti, seguendo le tendenze dell’obesità e del diabete. La gravità dei sintomi può variare da semplice steatosi, che è benigna e asintomatica, a steatoepatite non alcolica (NASH), che è caratterizzata da infiammazione del fegato, gonfiore e fibrosi e può portare a cirrosi e cancro al fegato.
Le persone che seguono una dieta ricca di grassi sono più sensibili alla NAFLD, e ciò è noto in ambito Pnei e fegato.
Replicando tale dieta nei topi, i ricercatori hanno scoperto che in poche settimane il loro microbiota intestinale ha cambiato le sue caratteristiche in modo significativo, con alcune specie di batteri in aumento e altre in diminuzione. Allo stesso tempo, un inventario dei metaboliti nel tratto gastrointestinale dei topi, nel siero e nel fegato, mostrava che alcuni metaboliti noti per essere collegati al microbiota intestinale erano ridotti rispetto ai topi alimentati con una dieta povera di grassi. Tre di questi metaboliti – triptamina (TA), indolo-3-acetato (I3A) e acido xanturenico – erano significativamente esauriti nei topi alimentati con dieta ricca di grassi.
La ricerca ha fornito conferme a quanto già noto nella metodologia Pneisystem in ambito di Pnei e fegato: lo studio infatti ha riscontrato come due di questi metaboliti – I3A e TA – siano in grado di attenuare gli effetti dell’infiammazione in diversi modi: il loro esaurimento spiana la strada alla progressione della malattia verso stadi più gravi.
Alcuni di quegli effetti di I3A e TA includono la riduzione del livello di molecole che inducono l’infiammazione (note come citochine) come il TNF-α, l’interleuchina-1-beta e la proteina chemoattrattiva del monocito. Quest’ultima funge da attrattiva per i macrofagi, che a loro volta producono più citochine. Ed i meccanismi di controllo delle citochine infiammatorie nella metodologia Pneisystem, e nel caso specifico secondo un approccio in Pnei e fegato e nelle terapie in chiave Pnei, riveste una conferma di rilevante importanza. Tutti questi agenti infiammatori sono innescati da alti livelli di accumulo di acidi grassi liberi nel siero e nel fegato – il segno distintivo della NAFLD e la conseguenza di una dieta ricca di grassi e insalubre.
I ricercatori hanno anche valutato se I3A e TA potrebbero essere aggiunti all’intestino per aiutare a trattare le fasi infiammatorie più gravi della NAFLD. Tuttavia, è stato determinato che alti livelli di TA sono tossici. Ora l’obiettivo futuro di questo studio prevede un focus dedicato su I3A, in particolare si valuterà se I3A o altri metaboliti del microbiota possano modificare il decorso della malattia.

 La chetogenica nella steatosi non alcolica
La chetogenica nella steatosi non alcolica Frutta e verdura per un fegato a posto
Frutta e verdura per un fegato a posto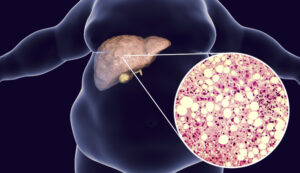 EpatosteatosiL'epatosteatosi, nota anche come fegato grasso, consiste in un eccessivo accumulo di grasso sotto forma di trigliceridi nelle cellule epatiche.
EpatosteatosiL'epatosteatosi, nota anche come fegato grasso, consiste in un eccessivo accumulo di grasso sotto forma di trigliceridi nelle cellule epatiche. Terapia funzionale in condizioni patologicheLa maggior parte delle patologie richiede una terapia dietetica mirata e una correzione dello stile di vita; la terapia deve essere personalizzata.
Terapia funzionale in condizioni patologicheLa maggior parte delle patologie richiede una terapia dietetica mirata e una correzione dello stile di vita; la terapia deve essere personalizzata.

